隨著生命科學研究的微觀化,基于細胞群體的研究方法已不適用于某些研究領域(如腫瘤異質性、早期胚胎發育等)。單細胞基因組測序通過在單個細胞水平上進行測序,解決了用組織樣本無法獲得不同細胞間的異質性信息或樣本量太少無法進行常規測序的難題,為科學家研究單個細胞的行為、機制等提供了新的方向。
【應用概覽】
從2011年Navin等人將全基因組擴增技術與高通量測序技術結合起來進行乳腺癌細胞研究開始,單細胞基因組測序技術已逐漸被應用于神經科學、生殖系演化、器官發生、腫瘤、臨床診斷、免疫學、微生物學、組織嵌合、胚胎發育以及產前遺傳學診斷等研究領域,并被《自然方法》雜志( Nature Methods )列入2013年度值得期待的技術之一。
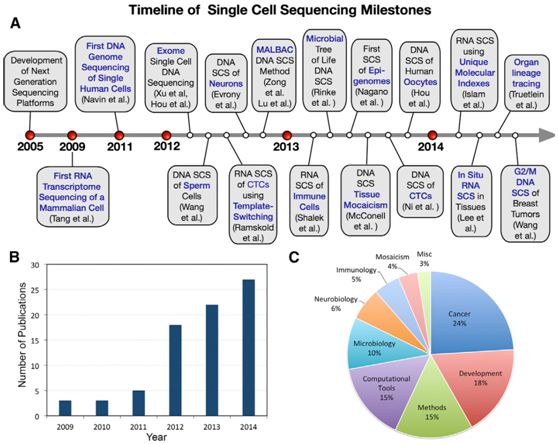
單細胞測序發展歷程及出版物數量和類目[1]
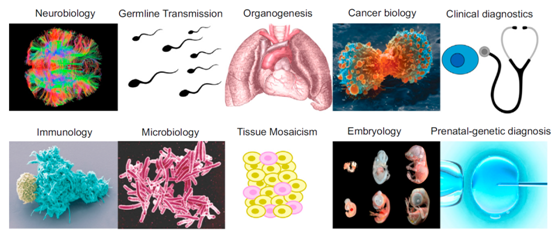
單細胞基因組測序技術被廣泛應用于生物科學和生物醫學領域[1]
【技術流程】
單細胞基因組測序主要包括四個步驟:單細胞分離→全基因組擴增→高通量測序→數據分析。其中,單細胞分離及全基因組擴增對最終結果的準確性起到了關鍵作用。
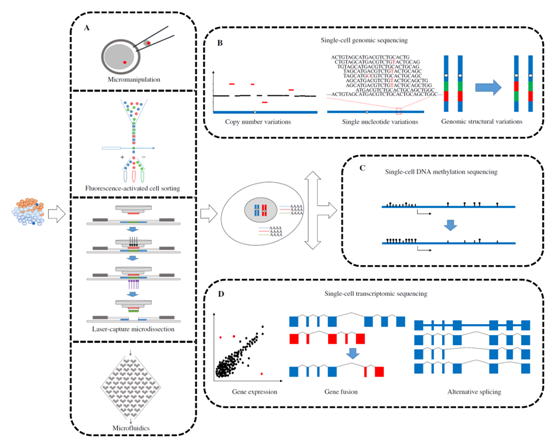
單細胞測序流程示意圖[2]
1. 單細胞分離
將單個細胞從組織中分離出來是單細胞基因組測序的第一步。雖然已有較成熟的用于分離在細胞群體中占多數的單細胞的技術,但分離在細胞群體中罕見(<1%)的單細胞仍是一項艱巨的挑戰。目前常用的單細胞分離方法主要有:毛細管吸取、流式細胞分選術、激光捕獲顯微切割技術(LCM)、微流控技術等。
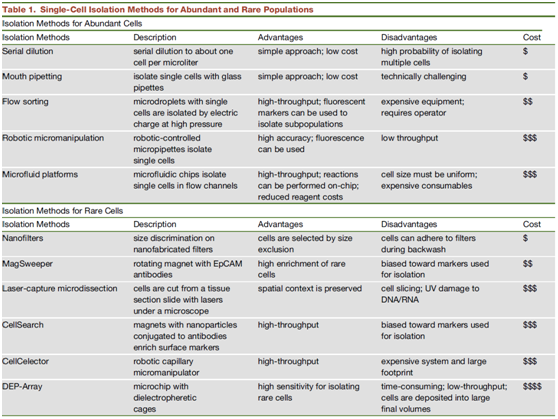
單細胞分離技術[1]
2. 全基因組擴增(WGA)
由于單細胞中DNA的含量非常小(約6pg/細胞),達不到測序儀的檢測要求,故在測序前,必須先對單細胞中的DNA進行擴增富集。現有的全基因組擴增方法按原理可分為三類:基于PCR的WGA方法、多重鏈置換擴增(MDA)、多次退火環狀循環擴增技術(MALBAC)。

幾種主要的全基因組擴增技術原理示意圖[3]
1) 基于PCR的WGA方法
基于PCR的WGA方法有很多種,如LA-PCR、PEP-PCR、DOP-PCR等。目前常用的是DOP-PCR和D-DOP-PCR,兩者都是通過加入隨機引物與模板結合的方式來達到擴增整個基因組的目的,不同之處主要在于后者所用的DNA聚合酶具有鏈置換功能。此類方法常見的商業試劑盒為:GenomePlex Single Cell Whole Genome Amplification Kit (Sigma-Aldrich, USA)和PicoPLEX WGA Kit (Rubicon Genomics, USA)。
2) MDA
MDA是一種滾環擴增技術,其原理主要是先讓DNA變性成單鏈,加入隨機引物與模板退火結合,再通過φ29 DNA聚合酶或Bst DNA聚合酶進行鏈置換合成反應使DNA擴增。標準的MDA實驗方案中采用的是φ29 DNA聚合酶,因為它相對Bst DNA聚合酶有更高的產量、保真性以及更低的擴增偏好性。其常見試劑盒為:REPLI-g Single Cell Kit (Qiagen, Germany)。
3) MALBAC
MALBAC通過特殊的隨機引物,使擴增產物首尾互補成環,進行近乎線性的全基因組預擴增,再通過PCR技術進行指數式擴增,從而降低擴增過程中錯誤累積。其常見試劑盒為:MALBAC Single Cell WGA Kit (Yikon Genomics, China)。
3. 高通量測序
自2005年454 Life Sciences公司(2007年被Roche正式收購)推出454 FLX焦磷酸測序平臺以來,高通量測序平臺不斷更新換代,但目前獲得國家食品藥品監督管理總局(CFDA)批準可用于臨床應用的二代測序儀只有國內少數幾家測序服務公司的Ion Proton(Life Technologies)、NextSeq 500(Illumina)等測序平臺。
Ion Proton和NextSeq 500都是采用邊合成邊測序(SBS)的測序原理,不同之處在于Ion Proton是以dNTP水解時釋放H+所導至的局部酸堿度變化為檢測信號,而NextSeq 500是以dNTP攜帶的熒光信號為檢測信號。
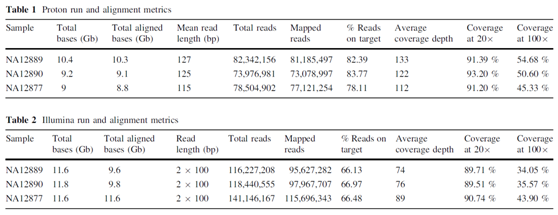
Ion Proton和Hiseq平臺測序結果比較[4]
4. 數據分析
數據分析基本流程
![]()
目前常見的變異類型為單核苷酸多態性(single nucleotide polymorphism, SNP)、插入缺失標記(insertion-deletion, InDel)和拷貝數變異(copy number variation, CNV)。
1) SNP、InDel
SNP和InDel是基因組上單個點或若干個(通常不大于30個)點上堿基的改變,在腫瘤、胚胎植入前遺傳學診斷(PGD)等領域較常見。目前大多數檢測效果較好的分析軟件都是先利用Genome Analysis Toolkit(GATK)初步檢測SNP或INDEL,再根據不同項目需求對檢測到的SNP和INDEL進行篩選,最后通過公共數據庫或本地數據庫對SNP和INDEL進行注釋。
2) CNV
CNV是一種基因組結構變異(SV),是由基因組發生重排而導至的基因組大片段(一般長度在1 kb 以上)拷貝數增加或者減少。CNV檢測目前在腫瘤發生及演化、神經元異質性研究、胚胎植入前篩查(PGS)等領域應用廣泛,但其檢測方法有很多,原理和流程也不盡相同。以目前熱門的PGS產品為例,CNV的檢測流程主要包括:將每條染色體分割為20kb連續的窗口→統計待測樣本序列中比對到各窗口中的唯一比對片段數→數據標準化→計算檢測指標→尋找斷點→篩選拷貝數變異。
【技術支持】
本專題資料由蘇州貝康醫療器械有限公司提供并參與校對。
蘇州貝康醫療器械有限公司(下稱貝康醫療)是一家專注于高通量測序技術在輔助生殖領域的研發和臨床應用的高科技企業。針對目前PGD/PGS存在的問題,貝康醫療研發了胚胎植入前染色體檢測試劑盒,基于高通量測序技術對體外受精的胚胎進行染色體檢測,挑選染色體正常的胚胎植入到子宮,以提高試管嬰兒的成功率。同時公司致力于該技術的臨床應用推廣,使更多的不孕不育患者受惠于此,特別是在目前中國二孩政策的前提下,對于降低出生缺陷,提高中國優生優育水平起到關鍵作用,可以降低老百姓生育缺陷兒的痛苦,提高中國人口質量。
參考文獻
1. Wang Y, Navin Nicholas E. Advances and Applications of Single-Cell Sequencing Technologies. Molecular Cell.58(4):598-609.
2. Liang J, Cai W, Sun Z. Single-Cell Sequencing Technologies: Current and Future. Journal of Genetics and Genomics. 2014;41(10):513-28.
3. Blainey PC. The future is now: single-cell genomics of bacteria and archaea. FEMS Microbiology Reviews. 2013;37(3):407-27.
4. Boland JF, Chung CC, Roberson D, Mitchell J, Zhang X, Im KM, et al. The new sequencer on the block: comparison of Life Technology’s Proton sequencer to an Illumina HiSeq for whole-exome sequencing. Human Genetics. 2013;132(10):1153-63.