1 簡介 本產品是用競爭酶聯免疫反應原理來檢測生物樣本中的氯霉素含量。本試劑盒包含檢測所需的所有試劑——包括標準品。 檢測數量:96孔(包括標準品) 檢測時間:20分鐘 2 應用范圍 本試劑盒可用于檢測奶、組織(肌肉、肝臟、腎臟、蝦類、蟹類、魚類)、尿液、血液和飼料樣本中的氯霉素。 3 原理 反應在包被了氯霉素抗體的固相微孔板上進行。標準品、樣品和酶標物加入到微孔中,第一次溫浴時,標準品或樣品中的游離氯霉素分子與酶標記的氯霉素分子競爭結合吸附在固相上的抗體結合位點。沒有結合的分子被清洗除去,通過加入顯色底物來確定已經結合的酶的活性,酶使得無色的底物轉變成蘭色,加入反應終止液使得蘭色變為黃色,用酶標儀在450nm處讀出吸光度。顏色的深淺可以轉換為樣品中氯霉素的不同濃度。 4 試劑組成 微孔板:96孔(12×8,可分拆)直接包被氯霉素抗體 標準品:0.025ng/mL; 0.1ng/mL; 0.25ng/mL; 1ng/mL; 4ng/mL; 1ml含0.1ug/ml濃度的氯霉素標準品1瓶 酶標物凍干粉:玻璃瓶 1瓶 酶標物稀釋液:13ml塑料瓶1瓶(棕色) 顯色劑:13ml 塑料瓶1瓶(棕色) 終止液:13ml塑料瓶1瓶(白色) 清洗液10×:50ml塑料瓶1瓶(白色) 氯霉素樣品稀釋液10×:50ml塑料瓶1瓶(白色) 5 需要但未提供的材料 樣品前處理需要: - 甲醇、乙酸乙酯、正己烷、異辛烷、三氯甲烷 - 組織勻漿機、天平、水浴鍋,搖床(振蕩器) - 離心機,氮吹儀,混合振蕩器 檢測中需要: - 20~200ul移液槍和槍頭 - 50~200ul多通道移液槍和槍頭 - 配備450nm濾光片的酶標儀 - 擠瓶 6 注意事項 - 終止液含有硫酸,注意不要接觸皮膚 - 顯色劑有毒,不要接觸皮膚;如果接觸請用水沖洗 - 不要在有效期過后使用試劑 - 不同批號的試劑不要混用 7 保存 - 2~8℃保存,切勿冰凍 - 沒有使用的微孔條請務必用干燥劑保存在密封的袋子中 8 樣品前處理 8.1尿樣 8.1.1直接法 — 200μl尿樣與800μl氯霉素樣品稀釋液混合 — 混合物在2000g,離心10min — 取50μl上清用于檢測 — 檢測最終結果應乘以稀釋倍數5 8.1.2抽提法 建議對“深色/不潔”尿樣采用 — 1ml尿液用1M乙酸調PH值到4.8 — 加入25μl蝸牛液(Helix pomatia juice),37℃下溫浴過夜或55℃下溫浴2小時。 — 冷卻至室溫,并將PH值調節到7±0.5 — 加入2ml乙酸乙酯,混合1min。靜置5-10 min分層。 — 將1ml上層液(乙酸乙酯層)轉移到干凈的試管中。 — 50℃,氮吹儀吹干 — 用200氯霉素樣品稀釋液溶解,混勻 — 取50μl用于檢測 — 檢測最終結果應乘以稀釋倍數0.4 8.2 血清/血漿樣品 — 1ml血清/血漿加入2ml乙酸乙酯混合1min,靜置5-10min,令其發生相分離 — 取1ml乙酸乙酯于一新的試管 — 50℃,氮吹儀吹干 — 加入500μl氯霉素樣品稀釋液混合均勻 — 取50μl用于檢測 — 檢測最終結果應乘以稀釋倍數1 8.3 奶 8.3.1 — 2000g,離心15min,去除上層脂肪 — 取50ul用于檢測。 注意:檢測酸奶時,應調樣品PH值至中性。 8.3.2 — 取5ml牛奶樣品于一試管中 — 2000g,離心15min,去除上層脂肪 — 取2.5ml脫脂奶于一新的試管 — 加入5ml乙酸乙酯,渦旋混合1min,靜置10min — 取4ml乙酸乙酯上層到干凈玻璃管中 — 50℃,氮吹儀吹干 — 用200μl氯霉素樣品稀釋液溶解 — 取50μl用于檢測 — 計算最終結果應乘以稀釋倍數0.1 (脫脂奶粉處理方法:將60ml蒸餾水加入10g脫脂奶粉,再按上述步驟操作) 8.4蛋類樣品 — 取1g勻漿全蛋 — 加入6ml乙酸乙酯渦旋混合1min — 2000g離心10min — 取3ml上層乙酸乙酯于一新的試管 — 50℃,氮吹儀吹干 — 加入1ml異辛烷/三氯甲烷(2:3,V/V),再加入500μl氯霉素樣品稀釋液,渦旋混合1min — 2000g,離心10min — 取50μl上層用于檢測 — 計算最終結果應乘以稀釋倍數1 注意:若上層乳化,可將試管置于80℃水浴約5min,并再次進行離心。 8.5 組織樣品(肉類、肝臟、蝦類、蟹類、魚類) 方法一: — 取3g勻漿樣品 — 加入6ml乙酸乙酯渦旋混合,振搖10min — 2000g,離心10min — 取4ml乙酸乙酯上層于一新的試管 — 50℃,氮吹儀吹干 — 加入1ml異辛烷/三氯甲烷(2:3,V/V),再加入1ml氯霉素樣品稀釋液,渦旋混合1min — 2000g,離心10min — 吸取50μl上層用于檢測。 — 計算最終結果應乘以稀釋倍數0.5 注意:若上層乳化,可將試管置于水浴(80℃ )約5min,并再次進行離心。 另:可以用正己烷代替異辛烷/三氯甲烷。若采用正己烷,離心后應完全去除上層正己烷,移取50μl下層用于檢測。 方法二:用于蝦、魚、蟹類的大樣品量處理 — 10g勻漿化樣品與20ml乙酸乙酯混合10min — 2000g,離心10min(或用濾紙過濾) — 取10ml乙酸乙酯層于一新的試管 — 50℃,氮吹儀吹干 — 加入2ml異辛烷/三氯甲烷(2:3,V/V)(或2ml正己烷,參見方法一),并加入1ml氯霉素樣品稀釋液,充分混合。若發現乳化,可將試管在水浴(80℃)中加熱(5min)。并將此溶液在2000g下離心10min。 — 利用巴斯德滴管轉移上層清夜(若用正己烷,清夜則在下層)于清潔玻璃管中。 — 再加入1ml異辛烷/三氯甲烷(2:3,V/V)(或1ml正己烷)。混合上述溶液并離心分離如上。 — 吸取50μl上層用于檢測(若用正己烷,清液則在下層)。 注:檢測最終結果乘以稀釋倍數0.2 8.6 蜂產品 8.6.1蜂蜜樣品 — 3g樣品與3ml蒸餾水充分混合 — 加入6ml乙酸乙酯充分振蕩混合10min — 2000g離心10min — 轉移4ml上層乙酸乙酯于一新的試管 — 50℃,氮吹儀吹干 — 殘留物充分溶解于1ml氯霉素樣品稀釋液 — 吸取50μl用于檢測 對于不純凈的蜂蜜應進行脫脂處理: — 將氮流蒸發后的殘留物溶于1ml異辛烷/三氯甲烷(2:3,V/V),加入1ml樣品稀釋液 — 渦旋混合1min,2000g,離心10min 注意:若上層乳化,可將試管置于水浴(80℃)約5min,并再次進行離心。 — 吸取50μl上層用于檢測。 — 檢測最終結果應乘以稀釋倍數0.5。 另:可以用正己烷代替異辛烷/三氯甲烷。若采用正己烷,離心后應完全去除上層正己烷層,移取50μl下層用于檢測。 8.6.2蜂王漿 — 1g蜂王漿與4ml抽提緩沖液(10.1g 1-庚烷磺酸,11.4g Na3PO4.12H2O。溶于1000ml蒸餾水中,用H3PO4調整pH2.0)混合30min — 3000g離心10min — 取2.5ml上清液用Oasis HLB柱(60mg Waters公司WAT094226)按以下固相抽提步驟純化: — 依次用1ml100%甲醇和1ml蒸餾水活化該柱(樣品過柱前柱不能過干,否則需要重復活化) — 將上述2.5ml上清液真空抽濾過柱 — 用3ml蒸餾水及3ml 50%(1:1;V:V)甲醇洗柱,真空干柱 — 用1ml100%甲醇洗脫,用干凈玻璃管收集洗脫液 — 洗脫液在溫和氮流下蒸發甲醇 — 樣品殘留物溶入0.5ml氯霉素樣品稀釋液中 — 吸取50μl用于檢測 — 檢測最終結果乘以稀釋倍數1 注意:若無真空泵,可使用正壓洗滌柱子; 流速均設定為1ml/min。 8.7 飼料樣品 — 5g樣品與20ml蒸餾水混勻 — 取5ml混合物到干凈玻管中,加入10ml乙酸乙酯混合2min — 2000g離心10min — 轉移5ml乙酸乙酯(上層)到干凈玻管中,50℃溫和的氮流下蒸發 — 殘留物溶于0.5ml異辛烷/三氯甲烷(2:3,V/V),加入0.5ml氯霉素樣品稀釋液,混合液渦旋1min, — 2000g離心10min — 取50μl上層用于檢測 — 檢測最終結果應乘以稀釋倍數1 注:若發現乳化,可將試管在水浴(80℃)中加熱(5min),并將此溶液再次離心,吸取50μl上層清液檢測 注意:本說明書提供的樣品前處理方法僅作參考,實驗人員可以根據自己的經驗作改善以提高檢測準確度。 9 工作液準備 為了避免污染,建議在配置標準品不要與試劑檢測工作在同一室內進行,并使用不同的移液槍。 注意:整套標準品應該在每個檢測實驗前臨時配置!! 氯霉素樣品稀釋液:用蒸餾水10倍稀釋(1+9),注意:如果出現結晶,請將溶液放于室溫下搖動,重新完全溶解。 標準品配制:使用已經稀釋的氯霉素樣品稀釋液。 - 10ng/ml濃度:100ng/ml原始濃度溶液100ul +稀釋液900ul(1:10) - 4ng/ml濃度:10ng/ml溶液400ul +稀釋液600ul(1:2.5) - 1ng/ml濃度:4ng/ml 溶液 200ul +稀釋液600ul(1:4) - 0.25ng/ml濃度:1ng/ml溶液200ul+稀釋液600ul(1:4) - 0.1ng/ml濃度:0.25ng/ml溶液400ul+稀釋液600ul(1:2.5) - 0.025ng/ml濃度:0.1ng/ml溶液200ul+稀釋液600ul(1:4) 此氯霉素樣品稀釋液也應當用于B0孔。 酶標物:實驗前用12mL酶標物稀釋液溶解,并充分混勻。靜置8小時(或過夜,但至少4小時),切勿渦旋混勻。 清洗液:用蒸餾水10倍稀釋(1+9)。注意:如果出現結晶,請將溶液放于室溫下搖動,重新完全溶解。 顯色劑:備用。 終止液:備用。 10 分析步驟 10.1 注意事項 - 使用前請將試劑盒恢復到室溫(20~25℃) - 使用后請立即將所有試劑放回2~8℃ - 請不要改動分析步驟,尤其: - 不要在低于20℃條件下溫浴 - 要使用準確和精確的移液槍和適合的槍頭 - 一旦開始實驗,完成所有步驟,不要中斷 - ELISA結果的重復性跟洗板的效果和一致性非常密切,請遵循操作方法 - 不同的樣品和標準品使用一次性槍頭以避免交叉污染 - 不要讓槍頭和微孔中的溶液或內避接觸 10.2 檢測程序 1. 用記錄表記錄B0,標準品和樣品的位置,要求做雙孔平行。 2. 加入標準品和樣品: -50ul氯霉素樣品稀釋液加入B0孔 -標準品或樣品50ul加入微孔 3. 用多通道移液槍在所有微孔中加入100ul酶標物溶液。 4. 晃動酶標板。 5. 室溫(20~25℃)下溫浴10min。溫浴過程中建議晃動酶標板2~3次。 6. 清洗步驟: - 倒去微孔中的溶液 - 用擠瓶將所有微孔加滿清洗液,然后倒去 - 在吸水紙上拍打除去殘留溶液 重復清洗四遍。 不要讓微孔干燥。 7. 用多通道移液槍在所有微孔中加入100ul反應液。 8. 輕輕晃動酶標板。 9. 室溫(20~25℃)下溫浴10min。 10. 用多通道移液槍在所有微孔中加入100ul的終止液。 11. 輕輕晃動酶標板。 12. 在450nm下檢測吸光度,結果在10min內讀取最佳,30min內有效。 11 結果計算 - 計算最大結合率(B0)、標準品和樣品的平均吸光度 - 根據以下公式來計算標準品和樣品的結合率
標準品(或樣品)吸光度 最大結合孔吸光度 - 根據標準品的B/B0值在半對數曲線中畫出標準曲線 - 獲得樣品的B/B0值后在標準曲線上可以得到對應的氯霉素濃度值ppb(ug/kg或ug/L),實際濃度還要乘上稀釋倍數。 12檢測下限 組織 0.1ng/g 尿液和奶樣 0.2ng/mL 13 特異性
| 分子 | 交叉反應% |
| 氯霉素 | 100 |
| 琥珀氯霉素 | 92 |
| 氯霉素-葡萄糖苷酸 | 57 |
| 阿莫西林 | < 0.1 |
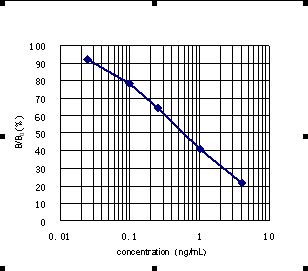
14標準曲線模型